Кеналог, Дипропан и другие кортикостероидные препараты быстро уменьшают воспаление, припухлость и отек. Однако они не излечивают артрит, не восстанавливают питание хряща и не улучшают состояние сустава. Они являются лишь экстренным средством — серьезным ударом по организму, особенно если такие методы лечения остеоартрита применяются слишком часто.
- Гормональные инъекции в суставы при остеоартрите: соглашаться или не соглашаться?
- Дозировка дексаметазона у собак
- Важность
- Характеристика препаратов ГКС и их потенциальные побочные эффекты
- Терапевтические режимы для ГКС
- Побочные эффекты краткосрочного лечения ГКС
- Заключение
- Источник финансирования
- Подробнее
Гормональные инъекции в суставы при остеоартрите: соглашаться или не соглашаться?
В последние годы ортопеды и ревматологи все чаще назначают пациентам инъекции в суставы. Этот метод привлекателен тем, что активное вещество быстро доставляется по «адресу» — в полость сустава. Препараты могут назначаться внутрь для уменьшения боли и воспаления, а также для восстановления хрящевой ткани и синовиальной жидкости. Иногда гормональные препараты входят в состав рецептов. Стоит ли соглашаться на такое лечение?
Инъекция гормонов в сустав быстро снимает боль
41. де Соуза Н. Г., Санта Марта К., Мораис-Алмейда М. Гиперчувствительность к системным кортикостероидам у детей. J. Investig. Аллергол. Клин. Иммунол. 2010;20:529-32.
Дозировка дексаметазона у собак
А. М. Сулейманова, Т. В. Куличенко
Национальный научно-практический центр здоровья детей, Министерство здравоохранения Российской Федерации, Москва
Важность
Эра широкого применения глюкокортикостероидов (ГКС) в клинической практике началась с первых исследований 1948 года, которые показали значительную эффективность применения кортизона у пациентов с ревматоидным артритом [1-3].
Многообразие физиологических эффектов и спектр фармакологического действия ГКС, включающий противовоспалительный, иммуносупрессивный, жаропонижающий, анальгетический, адаптогенный, неспецифический, стабилизирующий клеточные мембраны, противоотечный, противоаллергический, гематологический, гемодинамический, противосудорожный, антитоксический, противорвотный эффекты, определяют их разностороннее применение при различных патологических состояниях [1-4]. В клинической практике ГКС в основном используются в ревматологии, нефрологии, аллергологии, гематологии, трансплантологии и в чрезвычайных ситуациях. В связи с растущей распространенностью аутоиммунных и аллергических заболеваний использование ГКС в педиатрии в последние годы значительно возросло [4-6].
В настоящее время препараты ГКС широко доступны в пероральной, топической (для лечения кожных заболеваний), ингаляционной, интраназальной, внутрисуставной, офтальмологической, эпидуральной и парентеральной (внутривенной, внутримышечной) формах, а особенности их применения зависят от терапевтических стратегий, установленных клиницистами разных специальностей на основании нозологии [3-6].
Обладая широким спектром терапевтических свойств, ГКС неизбежно влияют на каждую из систем организма, что определяет не менее внушительный список потенциальных побочных эффектов их применения. Неблагоприятные последствия длительного, в течение десятилетий, лечения ГКС были предметом многочисленных исследований и подробно описаны в медицинской литературе [1-3]. Однако в современной педиатрической практике гораздо чаще встречаются короткие курсы лечения ГКС при различных острых состояниях. Безопасность краткосрочной терапии ГКС часто представляется как врачами, так и пациентами (или их родителями) как сравнимая с безопасностью длительного лечения этими препаратами. Стероидофобия довольно широко распространена как в медицинском сообществе, так и среди населения в целом. В некоторых случаях, наоборот, существует мнение об абсолютной «безвредности» кратковременного применения ГКС.
В отечественной литературе нет публикаций о безопасности краткосрочного использования ГКС в педиатрии.
Учитывая высокий спрос на препараты ГКС в клинической практике и необходимость адекватного понимания клиницистами потенциальных рисков, связанных с применением этих препаратов, целью данной работы был обзор опубликованных данных о безопасности краткосрочного лечения ГКС у детей с различными патологиями.
Источники данных включали публикации из PubMed, Cochrane Library, Medscape, e-library и монографии экспертов по данной теме.
Характеристика препаратов ГКС и их потенциальные побочные эффекты
Группа препаратов ГКС представлена эндогенными адренокортикоидными гормонами с преобладающей глюкокортикоидной функцией (кортизон и гидрокортизон) и их синтетическими аналогами (преднизон, преднизолон, метилпреднизолон), включая галогенизированные (фторированные) производные (триамцинолон, дексаметазон, бетаметазон) [1, 2]. В связи со значительными различиями в фармакокинетических и фармакодинамических свойствах ГКС важной задачей для клинициста является выбор препарата с наименьшим риском развития побочных эффектов (табл. 1). Учитывая оптимальное соотношение эффективности и безопасности, метилпреднизолон является препаратом выбора для длительного лечения. На данном этапе он широко используется в интенсивной терапии, аутоиммунных заболеваниях и трансплантологии. Универсальный состав позволяет использовать его во всех возрастных группах. В большинстве случаев преднизолон остается вторым по эффективности ГКС. Фторированные соединения, дексаметазон и бетаметазон, имеют некоторые преимущества (фармакокинетика, противовоспалительная активность) во многих чрезвычайных ситуациях (Таблица 1) [1, 2].

В зависимости от цели, варианты терапии ГКС различны, и лечение может быть как экстренным, так и элективным. ГКС обычно назначаются в качестве заместительной терапии при надпочечниковой недостаточности или с противовоспалительной и иммуносупрессивной целью (1-3). В отличие от обычной терапии, применение ГКС в чрезвычайных ситуациях обычно носит симптоматический, реже патогенетический характер, и не заменяет, а дополняет другие методы лечения. В неотложной терапии ГКС применяются при острой надпочечниковой недостаточности, тиреотоксическом кризе, аллергических заболеваниях (послеоперационные заболевания, анафилактический шок, бронхиальная астма, крапивница, отек Квинке). заболевания печени (печеночно-клеточная недостаточность), неврологические заболевания (туберкулез и бактериальный менингит, некоторые формы отека головного мозга), различные виды шока (кроме кардиогенного) [1-3].
Тщательный подбор препарата, режима дозирования и вида терапии не позволяет полностью предотвратить развитие побочных эффектов при применении ГКС (табл. 2).
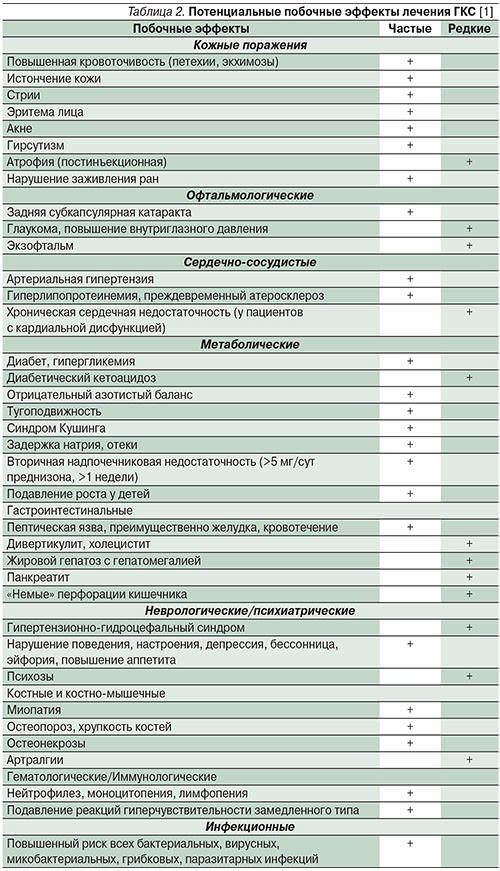
Развитие побочных эффектов ГКС может быть обусловлено следующими факторами [1-4]:
- Длительная и высокодозная терапия ГКС приводит к подавлению гипоталамо-гипофизарно-надпочечниковой регуляции, а ее прекращение связано с риском развития острой надпочечниковой недостаточности; Из-за противовоспалительного и иммуносупрессивного действия ГКС возможны атипичные инфекционные осложнения с тенденцией к генерализации, затяжным течением, разрушением тканей и устойчивостью к специфическому лечению. Стероидные язвы одинаково коварны, имеют бессимптомное течение, склонность к кровотечениям и перфорации. Однако диспепсические явления при лечении ГКС редко связаны с прямым повреждением слизистой оболочки желудочно-кишечного тракта; Возникновение метаболических и электролитных нарушений (синдром Кушинга, гипергликемия, остеопороз, повышение артериального давления) может быть связано с блокадой гормональной регуляции.
Терапевтические режимы для ГКС
Ввиду разнообразия побочных эффектов ГКС безопасность их применения в клинической практике зависит от определения строгих показаний к их назначению, оценки соотношения ожидаемого эффекта и воспринимаемого риска, а также своевременного предотвращения метаболических и электролитных нарушений.
Риск побочных эффектов ГКС зависит от следующих факторов [1]:
- Доза ГКС: 20 мг/сут — высокая доза; тип ГКС: длительного или короткого действия; Продолжительность лечения: длительное лечение >3 месяцев.
В зависимости от терапевтической стратегии можно выделить несколько схем ГКС [1-3]:
- Короткие курсы лечения высокими дозами с быстрой отменой препарата; Длительные курсы лечения малыми дозами и постепенная отмена препарата; пульс-терапия: интенсивное лечение с использованием очень высоких или средних/высоких доз; Альтернативная схема лечения.
Из-за широкого спектра потенциальных побочных эффектов терапия ГКС в первую очередь направлена на достижение максимального эффекта при минимальных дозах. Внутривенная пульс-терапия максимальными дозами считается наиболее эффективной, но и наиболее опасной (1-3). Следующими по эффективности методами являются чередующийся режим (двукратная ежедневная доза через день, затем постепенное снижение) и однократный ежедневный режим умеренной/высокой дозы. Терапия низкими дозами является наиболее безопасной, но обеспечивает лишь поддерживающий эффект (1-4). Во всех ежедневных схемах приема ГКС следует вводить рано утром (оптимально между 06:00 и 08:00); если однократный прием невозможен из-за размера дозы, 2/3 дозы следует вводить в 08:00, а 1/3 — во второй половине дня (около полудня). В обоих режимах дозирования после достижения желаемого эффекта дозу постепенно снижают до поддерживающей или вовсе прекращают прием препарата.
Выбор терапевтической схемы зависит от характера патологии. Короткие курсы ИКС обычно назначаются для лечения тяжелых и острых воспалительных состояний, таких как: лекарственная аллергия, контактный дерматит, тяжелый атопический дерматит, тяжелая крапивница, обострения бронхиальной астмы, воспалительные заболевания кишечника, ревматоидный артрит; различные гематологические заболевания [6-8]. Короткие курсы ГКС также используются (не всегда законно, конечно) в качестве терапии отчаяния или ex-uvantibus (7).
Лечение продолжительностью менее одного месяца считается краткосрочным. ГКС в течение нескольких дней или недель относительно безопасны. Лечение, продолжающееся более 3 месяцев, считается длительным и может привести к различным побочным эффектам [4, 5]. В обычной практике короткий курс ГКС соответствует применению преднизолона у взрослого человека в стандартной дозе 40-60 мг/сутки в течение от нескольких дней до 3 недель. Общая кумулятивная доза в таких случаях не превышает 600 мг, чаще она даже меньше 400 мг. У детей для краткосрочного лечения обычно используются дозы, соответствующие расчету 1-2 мг/кг массы тела преднизолона, при этом детям в возрасте 2-5 лет обычно назначают 20 мг/день [9]. Максимальная доза преднизолона у детей старшего возраста не должна превышать 60 мг/день (9).
Побочные эффекты краткосрочного лечения ГКС
Краткосрочное применение ГКС в целом считается безопасным. Однако минимальная доза системных ГКС и продолжительность приема, необходимые для возникновения побочных эффектов, не определены [6, 7]. Даже кратковременное применение препаратов ГКС следует рассматривать как потенциальный риск побочных эффектов.
В 2008 году Р. Ричардс опубликовал первый систематический обзор исследований, проведенных в период с 1985 по 2006 год, посвященных последствиям краткосрочного применения пероральных ИКС [7]. Проведенный анализ показал, что краткосрочный прием системных ГКС не связан с синдромом отмены; предпочтительным является однократный прием всей назначенной дозы ГКС с завтраком. Незначительные, редкие побочные эффекты включают бессонницу, перепады настроения, беспокойство, увеличение веса и несварение желудка (7).
Влияние на психологию. Влияние краткосрочного лечения ГКС на психику пациентов в связи с преобладанием этих эффектов при длительной терапии было предметом многих исследований. Значительные изменения настроения и психотические реакции очень редко наблюдаются при краткосрочном применении КОК (10-14). Исследования показывают, что пациенты, получающие суточную дозу преднизолона 40 мг или выше
Имеют более высокий риск психиатрических проблем (10,11). Симптомы могут появиться уже в первые дни лечения, а состояние психического здоровья пациента не является точным показателем развития побочных эффектов. Пациенты, получающие низкие дозы ИКС, имеют низкий риск развития тяжелых психических расстройств (10-14). Развитие побочных эффектов в этой области обычно связано с прекращением/снижением дозы ГКС и приемом фенотиазинов (10, 14).
Гипертония. Кратковременное применение ГКС обычно связано с клинически незначительным повышением артериального давления. Пациенты с тяжелыми заболеваниями сердца и/или сердечной недостаточностью нуждаются в тщательном наблюдении, чтобы избежать проблем с задержкой жидкости и соли. Любое снижение калия наряду с ГКС следует особенно тщательно контролировать у пациентов, принимающих дигоксин [15].
Повышенное внутриглазное давление. Обзор единичных сообщений о побочных эффектах свидетельствует о том, что пероральные ГКС могут приводить к повышению внутриглазного давления и глаукоме, однако влияние системных ГКС на глазное давление оценивалось только в одном исследовании [16]. Имеются данные о побочных эффектах при краткосрочном лечении глазными каплями, содержащими ГКС (16). На сегодняшний день нет опубликованных сообщений о глаукоме в результате краткосрочного лечения преднизолоном; однако из-за теоретической возможности развития глаукомы пациенты с глаукомой должны информировать своего офтальмолога при назначении системных ГКС и при необходимости контролировать глазное давление [16-18].
Гипергликемия. Прием ГКС может сопровождаться повышением уровня глюкозы в крови, поэтому у пациентов с диабетом следует контролировать уровень сахара в крови и при необходимости корректировать дозу инсулина (19). У пациентов без диабета гликемический контроль во время краткосрочного лечения системными ГКС обычно не требуется.
Пептические язвы. Пероральный прием ГКС может вызвать диспепсию, но одновременный прием с пищей может свести эти реакции к минимуму (20, 21). Причинная роль краткосрочного системного лечения ГКС в развитии язвенной болезни не доказана. Немногочисленные опубликованные сообщения о случаях заболевания, скорее всего, были связаны с одновременным применением нестероидных противовоспалительных препаратов (20).
Туберкулез. Пациенты, длительно принимающие НПВС, имеют повышенный риск первичной туберкулезной инфекции или реактивации, в то время как первичная туберкулезная инфекция не наблюдается при приеме препаратов короткого действия [22, 23].
Инфекционные заболевания. Более 20 лет назад A. E. Stuck и др. исследовали связь между терапией ГКС и последующим развитием инфекционных заболеваний путем мета-анализа данных контролируемых клинических испытаний. Они не обнаружили повышенного риска инфекционных осложнений при краткосрочном лечении ГКС у пациентов, получавших кумулятивную дозу преднизолона менее 700 мг (23).
В последние годы появляется все больше публикаций о возможности тяжелой или даже смертельной инфекции вирусом Herpes zoster во время или сразу после краткосрочного лечения ГКС. Известны случаи присоединения вируса ветряной оспы с вирусной диссеминацией, осложнениями и смертью при кратковременных ГКС в высоких дозах, у пациентов с ослабленным иммунитетом и у пациентов с обострением бронхиальной астмы [24-27].
Иммуносупрессивное действие ГКС может проявиться после 14 дней терапии ГКС или после дозы преднизолона 2 мг/кг/день (или >20 мг/день). В целом, более короткие курсы лечения не связаны с подавлением иммунитета (6, 7). Влияние на иммунитет нескольких повторных коротких курсов лечения ГКС в год не кажется клинически значимым, но это не было адекватно изучено (8).
Асептический некроз. Длительное применение системных ГКС может быть связано с развитием асептического некроза (28-30). Асептический некроз («аваскулярный остеонекроз») — это тяжелое дегенеративно-дистрофическое заболевание суставов, вызванное выраженной ишемией, сопровождающейся процессом некроза тканей сустава. Применение ГКС — не единственная возможная, но распространенная причина этого заболевания. Случаи некроза аспирина после лечения ГКС были описаны, когда кумулятивная (курсовая) доза преднизолона не превышала 290 мг (29).
Остеопороз. Остеопороз не связан с краткосрочным лечением ГКС, но профилактика, включающая прием кальция и холекальциферола, рекомендуется пациентам с высоким риском [7, 30].
Воздействие на плод. Исследования тератогенного действия ГКС классифицировали их риск как очень возможный (категория риска D), т. е. аномалии плода или другие необратимые повреждения могут наблюдаться с повышенной частотой при их использовании в первом триместре беременности (31). О серьезных последствиях для плода при последующем применении ГКС при беременности (категория риска С) не сообщалось (31). Преднизон оказывает наименьшее неблагоприятное воздействие на плод по сравнению с другими ГКС. Это связано с его фармакокинетическими свойствами: минимальное количество препарата в активной форме достигает кровообращения плода, поскольку плацента богата ферментом 11-β-гидроксистероиддегидрогеназой, который инактивирует преднизон (7, 31). Фторированные ГКС, такие как дексаметазон и бетаметазон, плохо преобразуются этим ферментом, поэтому их воздействие на плод может быть более серьезным. Преднизон выделяется в грудное молоко в минимальных количествах, поэтому Американская академия педиатрии пришла к выводу, что его прием совместим с грудным вскармливанием (32).
Анафилаксия. Имеются единичные сообщения об анафилактических реакциях, вызванных введением ГКС (33). Эрдманн и др. описали случай анафилаксии у 22-летней женщины с атопическим дерматитом, принимавшей перорально преднизон. Кожные тесты, проведенные впоследствии у пациента, показали немедленную гиперчувствительность к преднизолону, преднизону и бетаметазону и отсутствие гиперчувствительности к метилпреднизолону и дексаметазону [33].
Вакцинация и аллерген-специфическая иммунотерапия (АСИТ). Рекомендуется избегать введения живых вакцин детям во время лечения ГКС, поскольку иммуносупрессивный эффект ГКС может повысить риск развития побочных реакций (7). Живые вакцины против полиомиелита или кори/краснухи/паротита не следует вводить пациентам, принимающим ≥20 мг преднизолона в день (7). Другие обычные профилактические прививки, такие как ежегодная вакцинация против гриппа, безопасны и целесообразны.
Если пациент получает АСИТ и одновременно назначаются системные ГКС, иммунный ответ на лечение будет нормальным, если доза преднизолона не превышает 20 мг/день. Однако в большинстве случаев проведение АСИТ следует отложить до завершения лечения ГКС, поскольку более высокие дозы могут изменить результаты иммунизации [7, 33].
Длительное заживление ран. Обзор публикаций в области хирургии и дерматологии не выявил связи между короткими курсами ГКС и замедленным заживлением ран [6, 7].
Систематический обзор побочных эффектов. В 2016 году был опубликован мета-анализ исследований, анализирующих негативные последствия краткосрочного использования ГКС в педиатрии [6]. Всего в анализ было включено 3200 пациентов из 38 подходящих исследований, 22 из которых были рандомизированными. Короткие курсы лечения ГКС в основном применялись при синдроме крупа (обструктивный ларингит), обструктивном бронхите, аллергическом рините, обострении бронхиальной астмы, нефротическом синдроме, острой почечной недостаточности, лихорадке денге, судорожных расстройствах, остром лейкозе и системной красной волчанке [34-39]. Большинство детей получали преднизолон или дексаметазон. Всего было зарегистрировано 850 побочных реакций, связанных с ГКС. Наиболее распространенными были рвота (5,4%), поведенческие нарушения (4,7%) и нарушения сна (4,3%) [11, 12, 21, 40, 41]. Другие зарегистрированные побочные эффекты при краткосрочном лечении ГКС включали тошноту (1,9%), повышенный аппетит (1,7%), боль в животе (1,3%), отек и гиперемию лица (1,1%), инфекцию (0,9%) и кашель (0,2%) [6]. Из-за побочных эффектов препарат был отменен у 44 (1,4%) детей [6]. Мета-анализ показал, что наиболее серьезным побочным эффектом системных ИКС была инфекция, которая в одном случае привела к летальному исходу [26, 27]. В одном исследовании 144 (39%) из 369 детей сообщили о гипертонии, 21 (28%) из 75 детей — о наборе веса, а 43 (81%) из 53 детей — о подавлении функции гипоталамо-гипофизарно-надпочечниковой системы, диагностированном с помощью лабораторных тестов [42]. Все дети достигли нормальной секреции эндогенного кортизола в течение 10-12 дней после отмены ГКС. Исследователи отметили, что риск рвоты был в 3,6 раза выше при использовании преднизолона по сравнению с дексаметазоном [43].
Безопасность использования ГКС при обострениях бронхиальной астмы. Обострения бронхиальной астмы являются одной из наиболее распространенных причин назначения коротких курсов ИКС у детей. Обычно ГКС при обострениях астмы используются либо в виде 3-5 дневных курсов преднизолона 1-2 мг/кг/день или преднизона 1 мг/кг/день, либо в виде различных ингаляционных ГКС [44, 45]. Подавление надпочечников может быть продемонстрировано после двух месяцев непрерывного применения умеренной дозы (до 1 мг/кг/день) преднизолона или преднизона. Этот негативный эффект может сохраняться до одного года. После 5-дневного лечения преднизолоном или преднизоном в дозе 1-2 мг/кг/день подавления гипоталамо-гипофизарно-надпочечниковой функции не наблюдается (42). Кроме того, есть данные, что несколько повторных коротких курсов также не вызывают эндокринной недостаточности коры надпочечников (42). Однако следует отметить, что результаты этих исследований были получены на взрослых; их экстраполяция на детей сомнительна.
Семидневный курс системной терапии ГКС обычно не оказывает существенного влияния на функцию надпочечников, тогда как двухнедельный курс лечения высокими дозами может подавлять ее на срок до года (41). Следовательно, Национальные рекомендации по лечению острой бронхиальной астмы в настоящее время рекомендуют использовать пероральные ИКС в течение 3-7 дней, хотя предыдущие клинические рекомендации (2008) рекомендовали их использование в течение 7-14 дней [43, 44]. Кроме того, нет убедительных доказательств того, что другие пути введения препарата более безопасны, чем пероральный прием (1-3, 6, 41).
Ингаляционные ГКС, применяемые при бронхиальной астме, не вызывают неблагоприятных системных эффектов как при краткосрочном, так и при долгосрочном лечении низкими и умеренными дозами беклометазона пропионата (менее 0,5 мг/сут) [3, 5]. Сообщалось о подавлении надпочечников при длительном применении ингаляционных ГКС в дозах, превышающих 0,75-1,5 мг/сут беклометазона пропионата, и более высокий риск предполагается при использовании флутиказона [46].
Заключение
История использования ГКС при различных острых и хронических заболеваниях насчитывает несколько десятилетий. Эти препараты обладают уникальными свойствами, к которым в первую очередь относятся противовоспалительный и иммуносупрессивный эффекты. В связи с универсальностью ГКС спектр их побочных эффектов также широк. Развитие побочных реакций на ГКС напрямую связано с использованием высоких доз и длительностью терапии. Использование топических ГКС в последние годы значительно снизило частоту назначения системных ГКС и, соответственно, вероятность клинически значимых побочных реакций.
Длительное применение ИКС (курсы более 2 месяцев) связано как с подавлением функции надпочечников, так и с иммуносупрессией. Исследования показывают, что лечение короткими курсами системных ГКС (перорально 1-2 мг/кг/день преднизолона или преднизона в течение 3-7 дней) не вызывает таких эффектов, даже при использовании несколько раз в год. Однако несколько исследований показали, что увеличение продолжительности лечения системными ИКС свыше 7 дней повышает риск серьезных побочных эффектов.
Обзор литературы показал, что в целом короткие курсы лечения ИКС имеют удовлетворительный профиль безопасности. Наиболее распространенными побочными эффектами КОК в течение 7-14 дней являются диспепсия (тошнота, рвота), нарушения поведения и сна. В большинстве случаев эти же побочные эффекты приводят к отмене ГКС у детей. Применение системных ГКС в продромальный период ветряной оспы может быть наиболее опасным с точки зрения прогноза.
Возможные рекомендации по минимизации неблагоприятных эффектов системных ИКС заключаются в установлении четких критериев их назначения, сокращении длительности применения, если это возможно, и использовании наименьшей эффективной дозы.
Тщательное наблюдение за пациентами во время лечения, своевременное выявление факторов риска развития побочных эффектов и строгое соблюдение рекомендаций по рациональному назначению и применению этих препаратов — все это способствует более безопасной терапии ГКС и улучшению качества жизни пациентов.
Пациенты (или их родители), которым назначено краткосрочное лечение ГКС, должны быть проинформированы обо всех соответствующих рисках побочных эффектов и об альтернативных вариантах лечения.
Источник финансирования
Публикация подготовлена за счет собственных средств авторов.
Подробнее
1) Lin A. N., Paget S. A.. Принципы кортикостероидной терапии. Арнольд. 2002. 465 p.
2) Несбитт Л. Т. Глюкокортикостероиды. В: J. L. Bolognia, J. L. Jorizzo, R. P. Рапини, ред. Дерматология. Лондон: Мосби, 2003. P. 1979-89.
3 Городецкий В. В., Тополянский А. В., Лаптев А. О. Глюкокортикоидная терапия сегодня: эффективность и безопасность. https://www. lvrach. ru/2002/03/4529238.
4 Aljebab F., Choonara I., Conroy S. Систематический обзор токсичности длительного применения пероральных кортикостероидов у детей. PLoS One. 2017;12(1):e0170259.
5 Вознесенский Н. А., Поляков Д. П. Современные аспекты применения интраназальных кортикостероидов. Пульмонология и аллергология. 2010;1:20-4.
6 Aljebab F., Choonara I., Conroy S. Систематический обзор токсичности краткосрочного применения пероральных кортикостероидов у детей. Арх. Дис. Ребенок. 2016;101:365-70.
7 Richards R. N. Неблагоприятные последствия краткосрочного применения оральных кортикостероидов. J. Cutaneous Med. Хирургия. 2008;12(2):77-81.
8 Rieder M. J.. Ребенок с повторной кратковременной стероидной терапией. Pediatr. Ребенок. Здоровье. 2003;8(4):226.
9 Оказание стационарной помощи детям. Руководство по ведению наиболее распространенных заболеваний у детей. Карманный справочник, 2-е изд. Москва, 2013. 452 с.
10. Сируа Ф. Стероидный психоз: обзор. Hosp Gen. Психиатрия. 2003;25:27-33.
11. Холл А. С., Торли Г., Хоутман П. Н. Влияние кортикостероидов на поведение детей с нефротическим синдромом. Pediatr. Нефрол. 2003;18:1220-23.
12. Каяни С., Шеннон Д. К. Неблагоприятные поведенческие эффекты лечения острого обострения астмы у детей: сравнение двух доз пероральных стероидов. Грудь. 2002;122:624-28.
13. Доусон К. Л., Картер Э. Р. Стероид-индуцированный острый психоз у ребенка с астмой. Pediatr. Пульмонол. 1998;26:362-64.
14. Ularntinon S., Tzuang D., Dahl G., Shaw R. J. Одновременное лечение связанных со стероидами аффективных и психотических симптомов рисперидоном. Педиатрия. 2010;125:e1241-45.
15. Шолтер Д. Е., Армстронг П. В. Неблагоприятное воздействие кортикостероидов на сердечно-сосудистую систему. Can. J. Cardiol. 2000;16:505-9.
16. Beltrani V. S., Barsanti F. A., Bielory L. Эффекты глюкокортикостероидов на кожу и глаз. Иммунол. Allergy Clin. North. Am. 2005;25:557-80.
17. Carr W. W., Szefler S. J. Kortykosteroidy wziewne: Ocular safety and the hypothalamic-pituitary-adrenal axis. Ann. Allergy. Asthma Immunol. 2016;117(6):589-94.
18. Brito P. N., Silva S. E., Cotta J. S., et al. Severe ocular hypertension secondary to systemic corticosteroid treatment in a child with nephrotic syndrome. Клин. Ophthalmol. 2012;6:1675-79.
19. Braithwaite S. S., Barr W. G., Rahman A., Quddusi S. Управление диабетом во время глюкокортикоидной терапии. Jak uniknąć metabolicznych stanów nagłych. Diabetes. 1998;104:163-76.
20. Piper J. M., Ray W. A., Daugherty J. R., Griffin M. R. Применение кортикостероидов и язвенная болезнь: роль нестероидных противовоспалительных препаратов. Ann. Intern. Med. 1991;114:735-40.
21. Kim M. K., Yen K., Redman R. L., Nelson T. J., Brandos J., Hennes H. M. Рвота жидкими кортикостероидами у детей с астмой. Pediatr. Emerg. Care. 2006;22:397-401.
22. Chan Y. C., Yosipovitch G. Sugerowane wytyczne dotyczące badań przesiewowych i postępowania w gruźlicy u chorych przyjmujących doustne glikokortykoidy — ważne, ale często zaniedbywane zagadnienie. J. Am. Acad. Dermatol. 2003;49:91-5.
23. Stuck A. E., Minder C. E., Frey F. J. Риск инфекционных осложнений у пациентов, принимающих глюкокортикостероиды. Rev. Infect. Dis. 1989;11:954-63.
24. Hyvernat H., Roger P. M., Pereira C., et al. Смертельный гепатит ветряной оспы у взрослого астматика после краткосрочного лечения кортикостероидами. Eur. J. Intern. Med. 2005;16:361-62.
25. Hill G., Chauvenet A. R., Lovato J., McLean T. W. Недавняя стероидная терапия увеличивает тяжесть инфекций ветряной оспы у детей с острым лимфобластным лейкозом. Pediatrics 2005;116:525-29.
26. Kasper W. J., Howe P. M. Смертельная ветряная оспа после одного курса кортикостероидов. Pediatr. Infect. Dis. J. 1990;9:729-32.
27. Wu C.-T., Tsai S.-C., Lin J.-J., Hsia S. H. Диссеминированная инфекция ветряной оспы у ребенка, получающего краткосрочные стероиды для лечения астмы. Педиатрия. Dermatol. 2008;25:484-86.
28. Gebhard K. L., Maibach H. I. Взаимосвязь между системными кортикостероидами и остеонекрозом. Am. J. Clin. Dermatol. 2001;2:377-88.
29. McKee M. D., Waddell J. P., Kudo P. A., Schеmitsch E. H., Richards R. R. Osteonecrosis of the femoral head in men following short-course corticosteroid therapy: a report of 15 cases. CMAJ. 2001;164:205-6.
30. Richards R. N. Краткосрочные кортикостероиды и аваскулярный некроз: медицинские и юридические реалии. Cutis. 2007;80:343-48.
31. Gur C., Diav-Citrin O., Shechtman S., Arnon J., Ornoy A. Исход беременности после воздействия кортикостероидов в первом триместре: проспективное контролируемое исследование. Reprod. Toxicol. 2004;18:93-101.
32. Комитет по лекарствам Американской академии педиатрии. Передача лекарств и других химических веществ в человеческое молоко. Педиатрия. 1994;93:137-50.
33. Erdmann S. M., Abuzahra F., Merk H. F., Schroeder A., Baron J. M. Anaphylaxis induced by glucocorticoids. J. Am. Board. FAM Pract. 2005;18:143-46.
34. Rittichier K. K., Ledwith C. A. Амбулаторное лечение умеренного крупа дексаметазоном: внутримышечная и пероральная дозировка. Pediatrics. 2000;106:1344-48.
35. Head K., Chong L. Y., Hopkins C., Philpott C., Schilder A. G., Burton M. J. Short-course oral steroids as a adjunct therapy for chronic rhinosinusitis. Cochrane Database Syst. Rev. 2016;4:CD011992.
36. Chang A. B., Clark R., Sloots T. P., Stone D. G., Petsky H. L., Thearle D., Champion A. A., Wheeler C., Acworth J. P. 5- или 3-дневный курс оральных кортикостероидов для детей с обострениями астмы, которые не были госпитализированы: рандомизированное контролируемое исследование. Мед. J. 2008;189:306-10.
37. Panickar J., Lakhanpaul M., Lambert P. C., Kenia P., Stephenson T., Smyth A., Grigg J. Oral prednisolone for preschool children with acute virus-induced wheezing. N. Engl. J. Med. 2009;360:329-38.
38. Corneli H. M., Zorc J. J., Mahajan P., et al. A multicenter, randomized, controlled trial of dexamethasone for bronchiolitis. N. Engl. J. Med. 2007;357:331-39.
39. Tam D. T., Ngoc T. V., Tien N. T., Kieu N. T., Thuy T. T., Thanh L. T., Tam C. T., Truong N. T., Dung N. T., Qui P. T., Hien T. T., Farrar J. J., Simmons C. P., Wolbers M., Wills B. A. Эффект короткого курса пероральной кортикостероидной терапии на ранней стадии инфекции денге у вьетнамских пациентов: рандомизированное плацебо-контролируемое исследование. Clin. Infect. Dis. 2012;55:1216-24.
40. Vallance K., Liu W., Mandrell B. N., Panetta J. C., Gattuso J. S., Hockenberry M., Zupanec S., Yang L., Yang J., Hinds P. S. Mechanisms of dexamethasone-induced disturbed sleep and fatigue in paediatric patients receiving treatment for ALL. Eur. J. Cancer. 2010;46:1848-55.
41. де Соуза Н. Г., Санта-Марта К., Мораис-Алмейда М. Системная гиперчувствительность к кортикостероидам у детей. J. Investig. Allergol. Clin. Immunol. 2010;20:529-32.
42. Zora J. A., Zimmerman D., Carey T. L., O’Connell E. J., Yunginger J. W. Подавление гипоталамо-гипофизарно-надпочечниковой оси после краткосрочной высокодозной глюкокортикоидной терапии у детей с астмой. J. Allergy. Клин. Immunol. 1986;77:9-13.
43. Greenberg R. A., Kerby G., Roosevelt G. E. Сравнение перорального дексаметазона с пероральным преднизоном при обострениях астмы у детей, лечащихся в отделении неотложной помощи. Клин. Pediatr. (Phila). 2008;47:817-23.
44. Британское торакальное общество/Шотландская межвузовская сеть рекомендаций. British Guideline оn the Management of Asthma. 2014. https://www. brit-thoracic. org. uk/guidelines-and-quality-standards/asthma-guideline.
45. Douglas G., Higgins B., Barnes N., et al. British Guideline on the Management of Asthma (Brytyjskie wytyczne dotyczące postępowania w astmie). Thorax. 2008;63(Suppl. 4):71.
Читайте далее: