При применении SSRIs потеря веса ≥5 и ≥10% была достигнута у большего числа пациентов, получавших Оземпик® 0,5 мг (36 и 13%) и 1 мг (47 и 20%) по сравнению с пациентами, получавшими плацебо 0,5 мг (18 и 6%) и 1 мг (19 и 7%).
Ozempic®
Семаглутид — это агонист рецептора GFP-1 (GFP-1P), полученный биотехнологическим методом рекомбинантной ДНК с использованием штамма GFP-1P. Saccharomyces cerevisiae штамм с последующей очисткой.
Семаглутид — аналог GFP-1 с 94% гомологией с человеческим GFP-1. Семаглутид действует как агонист GTP-1P, который избирательно связывается с GTP-1P и активирует его. GTP-1R служит мишенью для нативного GTP-1.
GTP-1 — это физиологический гормон, который участвует в регуляции уровня глюкозы и аппетита, а также в работе сердечно-сосудистой системы. Воздействие на глюкозу и аппетит специфически опосредуется GFP-1P, расположенным в поджелудочной железе и мозге. Фармакологические концентрации семаглутида снижают уровень глюкозы в крови и массу тела за счет комбинации эффектов, описанных ниже. GTP-1R также присутствует в определенных областях сердца, кровеносных сосудов, иммунной системы и почек, где его активация может влиять на сердечно-сосудистую (СС) и микроциркуляцию.
В отличие от нативного GFP-1, расширенный T1/2 семаглутида (примерно 1 неделя) позволяет назначать его п/к один раз в неделю. Связывание с альбумином является основным механизмом длительного действия семаглутида, что приводит к снижению почечной экскреции и защите от метаболической деградации. Кроме того, семаглутид устойчив к расщеплению ферментом DPP-4. Семаглутид снижает уровень глюкозы в крови за счет глюкозозависимой стимуляции секреции инсулина и ингибирования секреции глюкагона. Таким образом, когда уровень глюкозы в крови повышается, секреция инсулина стимулируется, а секреция глюкагона подавляется. Механизм снижения гликемии также включает небольшую задержку опорожнения желудка в ранней постпрандиальной фазе. При гипогликемии семаглутид снижает секрецию инсулина и не снижает секрецию глюкагона.
Семаглутид снижает общую массу тела и массу жира за счет уменьшения потребления энергии. Этот механизм влияет на общее снижение аппетита, включая усиление сигналов сытости и снижение сигналов голода, а также улучшение контроля над потреблением пищи и снижение тяги к еде. Также снижается резистентность к инсулину, предположительно за счет снижения массы тела. Кроме того, семаглутид снижает предпочтение употребления продуктов с высоким содержанием жира. В исследованиях на животных было показано, что семаглутид поглощается определенными участками мозга и усиливает основные сигналы сытости и ослабляет основные сигналы голода. Воздействуя на изолированные участки мозговой ткани, семаглутид активирует нейроны, связанные с ощущением сытости, и подавляет нейроны, связанные с ощущением голода.
В клинических исследованиях (КИ) семаглутид оказывал благоприятное воздействие на уровень липидов в плазме крови, снижал САД и уменьшал воспаление.
В исследованиях на животных семаглутид препятствовал развитию атеросклероза, предотвращая дальнейший рост бляшек и уменьшая воспаление в атеросклеротических бляшках.
Фармакодинамические исследования
Все фармакодинамические исследования проводились после 12 недель лечения (включая период эскалации дозы) при Css семаглутид в дозе 1 мг один раз в неделю.
Уровень глюкозы в крови натощак и в постпрандиальный период
Семаглутид снижает уровень глюкозы натощак и постпрандиальный уровень глюкозы. По сравнению с плацебо, терапия семаглутидом (1 мг) у пациентов с сахарным диабетом 2 типа (СД2) привела к снижению уровня глюкозы в терминах абсолютного изменения от исходного уровня (ммоль/л) и относительного снижения по сравнению с плацебо (%) для быстрой глюкозы (1,6 ммоль/л); 22%), концентрация глюкозы через 2 часа после еды (4,1 ммоль/л; 37%), среднесуточная концентрация глюкозы (1,7 ммоль/л; 22%) и постпрандиальные пики глюкозы за 3 приема пищи (0,6-1,1 ммоль/л). Семаглутид снижал концентрацию глюкозы натощак после приема первой дозы.
Функция бета-клеток поджелудочной железы и секреция инсулина
Семаглутид улучшает функцию бета-клеток поджелудочной железы. После внутривенного введения реактивной глюкозы пациентам с СД2 семаглутид, по сравнению с плацебо, улучшал инсулиновый ответ первой и второй фазы, увеличивая его в три раза и в два раза, соответственно, и повышал максимальную секреторную активность панкреатических бета-клеток после теста стимуляции аргинином. Кроме того, по сравнению с плацебо, терапия семаглутидом повысила уровень быстрых инсулинов.
Секреция глюкагона
Семаглутид снижает концентрацию глюкагона натощак и постпрандиальную концентрацию глюкагона. У пациентов с СД2 семаглутид создает относительно более низкие концентрации глюкагона по сравнению с плацебо: концентрация глюкагона натощак (8-21%), постпрандиальный ответ глюкагона (14-15%) и среднесуточная концентрация глюкагона (12%).
Глюкозозависимая секреция инсулина и глюкозозависимая секреция глюкагона
Семаглутид снижал высокий уровень глюкозы в крови, стимулируя секрецию инсулина и снижая секрецию глюкагона глюкозозависимым образом. Скорость секреции инсулина после приема семаглутида у пациентов с T2DM была сопоставима со скоростью секреции инсулина у здоровых добровольцев.
Во время индуцированной гипогликемии семаглутид не изменял контррегуляторный ответ в виде повышения уровня глюкагона по сравнению с плацебо и не усугублял снижение уровня С-пептида у пациентов с СД2.
Опорожнение желудка
Семаглутид вызывал небольшую задержку раннего постпрандиального опорожнения желудка, тем самым снижая скорость постпрандиального всасывания глюкозы в кровь.
Масса тела и состав тела
При применении семаглутида наблюдалось более значительное снижение массы тела по сравнению с препаратами сравнения (плацебо, ситаглиптин, эксенатид с замедленным высвобождением (ER), дулаглутид и инсулин гларгин) (см. Клиническая эффективность и безопасностьЬ). Снижение веса после приема семаглутида происходило в основном за счет потери жира, превышающей потерю мышечной массы в 3 раза.
Аппетит, потребление калорий и выбор продуктов питания
По сравнению с плацебо, семаглутид снижал потребление калорий на 18-35% во время трех последовательных приемов пищи. По необходимости. В пользу этого говорит вызванное семаглутидом подавление аппетита как натощак, так и после еды, улучшение контроля над потреблением пищи и снижение тяги, особенно к продуктам с высоким содержанием жира.
Липиды натощак и постпрандиальные липиды
По сравнению с плацебо, семаглутид снизил уровень быстрых триглицеридов и Х-ЛПНП на 12% и 21%, соответственно. Постпрандиальное повышение уровня триглицеридов и hs-ЛПНП-C в ответ на прием пищи с высоким содержанием жиров было снижено более чем на 40%.
Электрофизиология сердца (ЭФС)
В исследовании ESF изучалось влияние семаглутида на реполяризацию в сердце. Применение семаглутида в дозах, превышающих терапевтические (при Css до 1,5 мг) не приводило к удлинению скорректированного интервала QT.
Клиническая эффективность и безопасность
Улучшение гликемического контроля и снижение сердечно-сосудистой заболеваемости и смертности являются неотъемлемой частью лечения СД2.
Эффективность и безопасность препарата Ozempic® в дозах 0,5 и 1 мг оценивались в 6 рандомизированных контролируемых исследованиях фазы 3a. Из них 5 КИ оценивали эффективность гликемического контроля в качестве первичной цели и 1 КИ оценивали СС исход в качестве первичной цели. Кроме того, было проведено 2 исследования фазы 3 препарата Ozempic® с участием японских пациентов.
Терапия Ozempic® продемонстрировала устойчивое, статистически значимое и клинически значимое улучшение показателей HbA1c и снижение веса на срок до 2 лет по сравнению с плацебо и лечением активными контрольными препаратами (ситаглиптин, инсулин гларгин, эксенатид ЗВ и дулаглутид).
Возраст, пол, раса, этническая принадлежность, исходный ИМТ и вес (кг), длительность сахарного диабета (СД) и почечной недостаточности не влияли на эффективность препарата Оземпик®.
Монотерапия
Монотерапия препаратом Оземпик® в дозе 0,5 и 1 мг один раз в неделю в течение 30 недель по сравнению с плацебо привела к статистически значимому снижению уровня HbA1c (-1,5; -1,6% против 0%, соответственно), концентрация глюкозы в плазме крови (FPG) (-2,5; -2,3 ммоль/л против -0,6 ммоль/л, соответственно) и масса тела (-3,7; -4,5 кг против -1 кг, соответственно).
Оземпик® по сравнению с ситаглиптином, оба в комбинации с 1-2 пероральными гипогликемическими препаратами (ПГП) (метформин и/или тиазолидиндионы).
Лечение препаратом Ozempic® в дозах 0,5 и 1 мг один раз в неделю в течение 56 недель по сравнению с ситаглиптином привело к устойчивому и статистически более значительному снижению уровня HbA1c (-1,3; -1,6% против -0,5%, соответственно), HbA (-2,1; -2,6 ммоль/л против -1,1 ммоль/л, соответственно) и масса тела (-4,3; -6,1 кг против -1,9 кг, соответственно). Терапия препаратом Ozempic® в дозе 0,5 и 1 мг по сравнению с ситаглиптином значительно снизила САГ с исходного уровня 132,6 мм рт. ст. (-5,1; -5,6 мм рт. ст. против -2,3 мм рт. ст., соответственно). Изменений в dAP не наблюдалось.
Оземпик® по сравнению с дулаглутидом, оба в комбинации с метформином
Лечение препаратом Ozempic® 0,5 мг по сравнению с дулаглутидом 0,75 мг, оба препарата принимались один раз в неделю в течение 40 недель, привело к устойчивому и статистически значимому снижению уровня HbA1c(-1,5 против -1,1%), ГПД (-2,2 против -1,9 ммоль/л) и масса тела (-4,6 против -2,3 кг).
Лечение препаратом Ozempic® 1 мг в сравнении с дулаглутидом 1,5 мг один раз в неделю в течение 40 недель привело к устойчивому и статистически значимому снижению уровня HbA1c(-1,8 против -1,4%), HbA (-2,8 против -2,2 ммоль/л) и масса тела (-6,5 против -3,0 кг).
Оземпик® против эксенатида ST, оба в комбинации с метформином или метформином в комбинации с производным сульфонилмочевины
Лечение препаратом Ozempic® в дозе 1 мг один раз в неделю в течение 56 недель по сравнению с эксенатидом SG в дозе 2,0 мг привело к устойчивому и статистически более значительному снижению уровня HbA1c(-l,5 против -0,9%), HbA (-2,8 против -2,0 ммоль/л) и масса тела (-5,6 против -1,9 кг).
Оземпик® по сравнению с инсулином гларгин, оба в комбинации с 1-2 ГГП (монотерапия метформином или метформин с производным сульфонилмочевины)
Лечение препаратом Оземпик® в дозе 0,5 и 1 мг один раз в неделю по сравнению с инсулином гларгин в течение 30 недель привело к статистически значимому снижению уровня HbA1c(-l.2; -1.6% против -0.8%, соответственно) и массы тела (-3.5; -5.2 кг против 1.2 кг, соответственно).
Снижение ГПД было статистически более значимым для Оземпик® 1 мг по сравнению с инсулином гларгин (-2,7 против -2,1 ммоль/л). При приеме Оземпика® 0,5 мг статистически значимого снижения ГПД не наблюдалось (-2,0 против -2,1 ммоль/л).
Доля пациентов с тяжелыми или подтвержденными (
Больше пациентов достигли уровня HbA1c
Оземпик® по сравнению с плацебо, в обоих случаях в комбинации с базальным инсулином.
Лечение препаратом Ozempic® в дозе 0,5 и 1 мг по сравнению с плацебо в течение 30 недель привело к статистически значимому снижению уровня HbA1c(-l.4; -1.8% против -0.1%, соответственно), HbA 1c (-1.6; -2.4 ммоль/л против -0.5 ммоль/л, соответственно) и масса тела (-3.7; -6.4 кг против -1.4 кг, соответственно). Частота тяжелых или подтвержденных гипогликемических эпизодов существенно не отличалась между Оземпиком® и плацебо. Процент пациентов с HbA1c ≤8% при скрининге, сообщения о тяжелых или подтвержденных (1c>8% при скрининге.
Монотерапия комбинацией производных сульфонилмочевины
Подгруппа из 123 пациентов, принимавших монотерапию производными сульфонилмочевины, была оценена после 30 недель наблюдения (см. «Оценка влияния ССС»). На 30-й неделе HbA1с снизился на 1,6 и 1,5% при применении препарата Оземпик® в дозах 0,5 и 1 мг, соответственно, и увеличился на 0,1% при применении плацебо.
Комбинация с инсулиновой смесью ±1-2 PGCP
Подгруппа из 867 пациентов, предварительно получавших смешанную инсулинотерапию (с 2 ПГКП или без них), была оценена на 30-й неделе КИ (см. в подразделе «Оценка влияния на ССС». На 30-й неделе HbA1c снизился на 1,3 и 1,8% при применении препарата Оземпик® в дозах 0,5 и 1 мг, соответственно, и снизился на 0,4% при применении плацебо.
Процент пациентов, достигших целевого снижения уровня HbA1c
До 79% пациентов достигли целевых показателей лечения по HbA1c
Процент пациентов, достигших уровня HbA1c менее 7% без тяжелых или подтвержденных гипогликемических эпизодов и без увеличения веса была значительно выше при приеме Оземпик® 0,5 и 1 мг (до 66 и 74%, соответственно) по сравнению с пациентами, получавшими ситаглиптин (27%), эксенатид ST (29%), инсулин гларгин (16%), дулаглутид 0,75 мг (44%) и дулаглутид 1,5 мг (58%).
Монотерапия Оземпиком® 1 мг или терапия в комбинации с 1-2 препаратами приводила к статистически более значительной потере веса (до 6,5 кг) по сравнению с плацебо, ситаглиптином, эксенатидом ZV, инсулином гларгин или дулаглутидом. Снижение веса сохранялось в течение 2 лет.
После одного года терапии большее число пациентов, получавших Оземпик® в дозе 0,5 мг (46 и 13%) и 1 мг (до 62 и 24%), достигли снижения веса на ≥5 и ≥10% по сравнению с пациентами, получавшими активные препараты сравнения ситаглиптин и эксенатид ЗВ (до 18 и 4%).
При 40-недельном наблюдении большее число пациентов, принимавших Ozempic® 0,5 мг (44 и 14%), достигли снижения веса на ≥5 и ≥10% по сравнению с пациентами, принимавшими дулаглутид 0,75 мг (23 и 3%). Снижение веса ≥5 и ≥10% было достигнуто большим количеством пациентов, получавших Оземпик® 1 мг (до 63 и 27%) по сравнению с пациентами, получавшими дулаглутид 1,5 мг (30 и 8%).
В CCI снижение веса на ≥5 и ≥10% было достигнуто большим количеством пациентов, получавших Оземпик® 0,5 мг (36 и 13%) и 1 мг (47 и 20%) по сравнению с пациентами, получавшими плацебо 0,5 мг (18 и 6%) и 1 мг (19 и 7%).
Препрандиальное и постпрандиальное повышение уровня глюкозы
При всех 3 приемах пищи в день Оземпик® 0,5 и 1 мг показал значительное снижение ГПД до 2,8 ммоль/л и снижение постпрандиального повышения глюкозы до 1,2 ммоль/л (разница между до — и постпрандиальными значениями после 3 приемов пищи) (дополнительно см. раздел «Фармакодинамические исследования»).
Функция бета-клеток поджелудочной железы и инсулинорезистентность
Во время лечения препаратом Оземпик® в дозе 0,5 и 1 мг функция бета-клеток поджелудочной железы и инсулинорезистентность снижались, что оценивалось с помощью гомеостатических моделей функции бета-клеток поджелудочной железы (NOMA-B) и инсулинорезистентности (HOMA-IR) (подробнее см. раздел «Фармакодинамические исследования»).
В ходе клинического исследования Ozempic® наблюдалось улучшение липидного профиля крови натощак, в основном в группе, принимавшей дозу 1 мг (дополнительно см. раздел «Фармакодинамические исследования»). «Фармакодинамические исследования»).
Оценка влияния на ССЗ
3 297 пациентов с T2DM и высоким риском СС были рандомизированы в двойном слепом 104-недельном исследовании для получения Ozempic® 0,5 или 1 мг один раз в неделю или плацебо 0,5 или 1 мг в дополнение к стандартной терапии заболевания СС в течение последующих 2 лет.
Терапия препаратом Оземпик® привела к снижению риска первичного комбинированного исхода на 26%, включая смерть от сердечно-сосудистых заболеваний, несмертельный инфаркт миокарда и несмертельный инсульт. Это было обусловлено, прежде всего, значительным снижением частоты нефатального инсульта (39%) и небольшим снижением частоты нефатального инфаркта миокарда (26%), но отсутствием изменений в частоте сердечно-сосудистой смерти.
Риск реваскуляризации миокарда или периферических артерий значительно снизился, а риск нестабильной стенокардии, требующей госпитализации, и риск госпитализации по поводу сердечной недостаточности снизился незначительно. Микрососудистые исходы включали 158 новых или ухудшившихся случаев нефропатии. ОР для времени до развития нефропатии (новые случаи стойкой макроальбуминурии, стойкое удвоение сывороточного креатинина, необходимость в постоянной заместительной почечной терапии и смерть от заболевания почек) составил 0,64.
В дополнение к стандартной терапии заболевания СС, терапия препаратом Osempic® в дозах 0,5 и 1 мг по сравнению с плацебо 0,5 и 1 мг в течение 104 недель привела к значительному и устойчивому снижению уровня HbA1c(-1,1 и -1,4% против -0,4 и -0,4%, соответственно).
Значительное снижение среднего значения MAP наблюдалось при использовании Оземпик® 0,5 мг (3,5-5,1 мм рт. ст.) и Оземпик® 1 мг (5,4-7,3 мм рт. ст.) в сочетании с ПГКП или базальным инсулином. Существенной разницы в уровне dAP между препаратом Оземпик® и препаратами сравнения не было.
Введение препарата в организм животного с помощью шприца является наиболее удобным и надежным способом
Тронцил-К: состав, лекарственная форма и условия хранения
Тронцил-К назначают кошкам для уничтожения гельминтов круглого и ленточного типа. Действующие вещества — празиквантел и пирантел. Кроме того, в состав композиции входят такие вещества, как:
- лактоза; микрокристаллическая целлюлоза поливинилпирролидон; стеарат магния; лаурилсульфат натрия; аэросил; картофельный крахмал.
Препарат выпускается только в виде таблеток; других форм не существует. Препарат следует хранить в прохладном месте, температура воздуха не должна превышать 20 градусов Цельсия. Срок годности составляет 5 лет.

Тронцил-К используется для уничтожения глистов у кошек.
Дегельминтизация домашних животных должна проводиться не реже трех раз в год. Вы можете начать с котенка в возрасте трех недель. Однако для этих целей следует использовать только специализированные препараты, такие как Тронцил-К и его аналоги. Важно соблюдать дозировку, иначе такое лечение может негативно сказаться на здоровье животного.
Срок годности Тронцил-К составляет 5 лет с даты изготовления.
Дозировка и применение препарата Тронцил-К
Для лечения глистных инвазий препарат применяется однократно. Дозировка зависит от веса кошки. В профилактических целях прием препарата повторяют каждые три месяца, дозировка та же. При выборе даты профилактической дозировки не следует нарушать рекомендованные сроки, но необходимо учитывать время планируемой вакцинации — дегельминтизацию проводят за две недели до вакцинации.
Таблица: Расчет дозы
| Вес кошки, кг | Дозировка, в таблетках |
| До 1 | 1/4 |
| 1–2 | 1/2 |
| 2–3 | 3/4 |
| 3–4 | 1 |
| 4–5 | 1+1/4 |
Перед применением препарата не требуется диета или голодание. Человек, работающий с таблетками, должен соблюдать правила личной гигиены, использование перчаток не обязательно.
Таблетку можно давать с пищей: растолочь и смешать с мясным фаршем, творогом или порцией паштета. Однако самым безопасным и быстрым способом введения лекарства является принудительное кормление:
Зафиксируйте тело кошки, чтобы она не могла царапаться или кусаться. Вы можете плотно обернуть его полотенцем. Двумя пальцами разожмите челюсти кошки, надавливая на уголки рта. Поместите таблетку на язык как можно дальше. Сожмите челюсти и поглаживайте шею кошки движениями вниз, провоцируя глотательный рефлекс. Затем вы можете дать кошке воду для питья или лакомство.
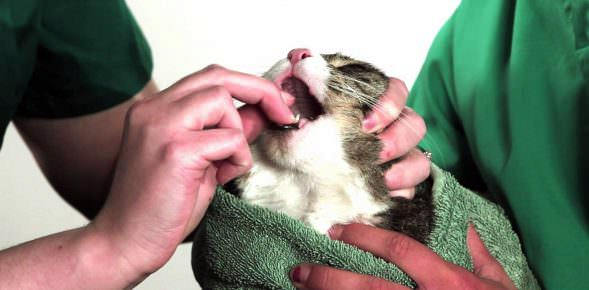
Таблетку следует положить как можно ниже к основанию языка, чтобы кошка не выплюнула ее.
Видео: как дать таблетку кошке
Дополнительные ингредиенты лекарства: картофельный крахмал, микрокристаллическая целлюлоза, лаурилсульфат натрия, лактоза, стеарат натрия.
Как действует Тронцил для собак от паразитов?
Тронцил — противопаразитарный препарат широкого спектра действия. Его производит московская компания «Ветбиохим», которая разрабатывает различные противопаразитарные и противоинфекционные средства для мелких домашних и сельскохозяйственных животных.
Активные вещества этого препарата оказывают комплексное губительное воздействие на гельминтов:
- вмешиваются в синтез АТФ; замедляют транспорт глюкозы; нарушают внутрисосудистый транспорт веществ; повышают проницаемость мембраны для определенных электролитов.
Все эти процессы приводят к нарушению нервной проводимости, сокращению мышечной ткани. Происходит паралич и гибель гельминта. Препарат эффективен против паразитов на любой стадии их жизненного цикла.
Препарат Фебантел, помимо действия на гельминтов, также обладает антипротозойным эффектом и применяется при лямблиозе у животных.
После приема активные вещества выводятся с фекалиями и мочой. Только празиквантел всасывается в кишечнике, после чего распределяется в кровотоке между органами и тканями, действуя терапевтически в течение 48 часов. Остальные компоненты практически полностью проходят через желудочно-кишечный тракт в неизменном виде.
Чтобы предотвратить прорастание этих «семян», домашних животных необходимо защищать от паразитов, уничтожая уже появившихся или предотвращая появление возможных паразитов.
Инструкция по применению Тронцил-К для кошек
Препарат вводится однократно, либо насильно, либо с пищей.
Для профилактики гельминтозов рекомендуется применять Тронцил-К каждые три месяца.
Дозировка
Как использовать Troncil для кошек? Для правильной дозировки необходимо знать точный вес вашего питомца.
- Если вес вашей кошки меньше килограмма, правильная дозировка — четверть таблетки Тронцил-К. Если ваш питомец весит до 1 кг — 2 кг, половину таблетки. От 2 до 3 кг — 3/4 таблетки. Полная таблетка дается, когда животное весит 3-4 кг.
Хранение
Тронцил-К является умеренно безопасным препаратом, поэтому его следует хранить в недоступном для детей и домашних животных месте. Температура хранения — 0 — 20 градусов Цельсия. Гарантийный срок хранения — 5 лет.
Читайте также. Другие препараты против глистов.
Читайте далее: